近日,江西農業(yè)大學豬遺傳改良與種質創(chuàng)新全國重點實驗室黃路生院士團隊在國際知名學術期刊《National Science Review》(五年影響因子17.7)發(fā)表了題為“Microglial function alterations during healthy ageing and canine cognitive dysfunction revealed by single-nucleus and spatial transcriptomics”的重要研究成果。該成果系統(tǒng)研究了健康衰老與老年癡呆認知障礙犬的腦細胞轉錄組,揭示了認知障礙犬中小膠質細胞C1QA與神經元CRT互作介導突觸損傷的新機制。
我校楊思雨博士后(兼第一作者)、景琦琦博士(兼共同第一作者,山東畜牧獸醫(yī)職業(yè)學院)與黃路生院士為通訊作者。

研究背景:
截至2024年統(tǒng)計數據顯示,全球阿爾茨海默病(AD)患者人數已逾5500萬(阿爾茨海默病協(xié)會,2024)。我國目前AD患者約983萬,平均每10位65歲以上的老年人中即有1人患病(中國阿爾茨海默病報,2024)。作為老年期最常見的癡呆類型,AD以腦內β-淀粉樣蛋白(Aβ)沉積和神經原纖維纏結為核心病理特征,是導致認知功能進行性喪失的主要原因之一。迄今該病的分子機制尚未完全闡明,因此缺乏有效治療手段,對醫(yī)療衛(wèi)生、家庭照護及社會經濟均構成沉重負擔。
目前,AD研究主要依賴嚙齒類動物小鼠或大鼠作為模式生物。這類動物因其體型較小、易于進行基因操作等優(yōu)勢,常被用于構建過表達家族性AD相關基因突變的轉基因小鼠模型(如3×Tg和5×FAD),以模擬部分病理過程(Michael Z.等,2024)。然而,由于小鼠壽命較短、神經解剖結構相對簡單,加之現有AD轉基因模型在病理生理特征方面與人類患者存在顯著差異,該類模型難以全面模擬人類AD的自然發(fā)病與發(fā)展過程(Zhengjiang等,2024)。這一局限性嚴重制約了AD機制研究的深入以及有效治療策略的研發(fā)。
相比之下,大型動物模型(如豬和犬)在腦結構與功能方面與人類更具保守性:它們具有類似的腦溝回結構和保守的靜息態(tài)網絡組織(Joan K.等,2021),近年研究還提示其在細胞類型特異性轉錄組層面也具有顯著的跨物種相似性(Siyu等,2023)。基于上述背景,本研究團隊以“一豬兩用”為核心策略,致力于構建能夠更準確模擬人類AD病理特征與臨床表現的豬/犬類大動物模型,以推動相關轉化醫(yī)學研究的發(fā)展。
在研究老年癡呆大動物模型過程中,研究團隊發(fā)現犬類作為與人類共享生活環(huán)境的伴生物種,不僅衰老過程與人類相似,還可自發(fā)出現犬認知障礙綜合征(CCD)(Alexandra A.等,2023)。該綜合征在病理上表現為Aβ斑塊和NFT形成,在行為特征方面也與人類AD高度接近,約22%的老年犬會罹患CCD(Alexandra A.等,2023),因此被視為研究AD及衰老機制的理想自然模型之一。因此,本研究通過獲得因自然死亡而自愿捐贈的CCD犬只樣本,并結合老年實驗犬設計研究方案,旨在利用這一自發(fā)模型推動AD病理機制與干預策略研究。
主要研究內容:
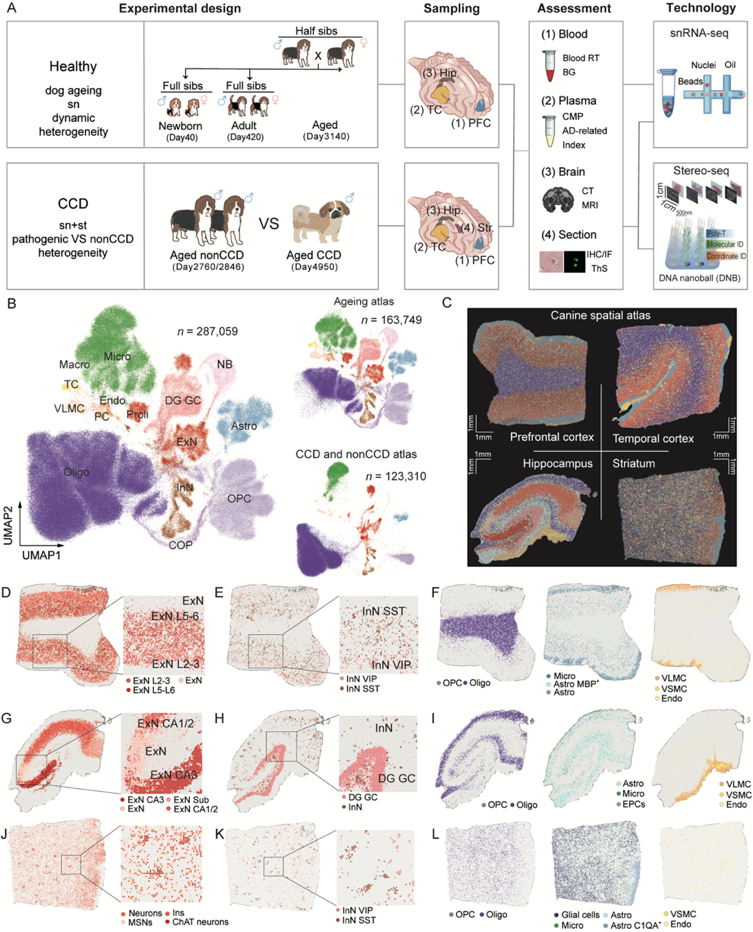
研究團隊首先利用單核RNA測序(snRNA-seq)和空間轉錄組(Stereo-seq)技術,構建了健康衰老大腦的單核轉錄組圖譜,以及CCD與非CCD犬大腦的對比性單核與空間轉錄組圖譜。基于上述圖譜,分別開展了以下分析:(1)正常衰老過程中不同細胞類型的轉錄動態(tài)變化;(2)CCD與非CCD犬大腦的病理機制差異分析;(3)正常衰老與CCD相關病理性衰老的分子特征比較,特別關注小膠質細胞在這兩種狀態(tài)下的共同與特異性變化。
通過對健康衰老圖譜的分析,研究團隊發(fā)現膠質細胞在衰老過程中表現出顯著的轉錄可塑性。線性回歸分析顯示,膠質細胞——尤其是少突膠質細胞、小膠質細胞和星形膠質細胞——隨衰老發(fā)生明顯的轉錄重編程。進一步針對這三類細胞的亞型分析,鑒定并驗證了兩種此前未被報道的衰老相關亞型:小膠質細胞中的Micro MBP?亞型與星形膠質細胞中的Astro MBP?亞型,二者均參與髓鞘合成過程。此外,在少突膠質細胞中鑒定出轉錄因子ZEB1,其表達隨衰老逐漸下降,該因子調控少突膠質細胞的分化,這一發(fā)現此前尚未被報道。
基于CCD與nonCCD犬的比較圖譜,團隊進一步探究了CCD的致病機制。通過snRNA-seq數據發(fā)現,在CCD犬中,小膠質細胞來源的C1QA與海馬神經元中的CRT發(fā)生相互作用,介導突觸損傷。該互作關系首先通過空間轉錄組數據得以驗證,進一步通過細胞共培養(yǎng)實驗證實:C1QA與CRT的相互作用可導致突觸標志物SYN1表達顯著下降,從而明確了該分子機制。
為區(qū)分健康衰老與CCD的分子差異,研究團隊系統(tǒng)篩選了AD相關風險基因集,并分析其在不同細胞類型衰老過程中的表達模式。結果顯示,多數AD風險基因在小膠質細胞中高度表達。進一步比較小膠質細胞在正常衰老與CCD狀態(tài)下的轉錄動態(tài),發(fā)現CCD犬的小膠質細胞代謝淀粉樣前體蛋白的能力明顯低于正常衰老犬,提示其功能退化可能與CCD的病理機制密切相關。
研究意義:
研究團隊創(chuàng)新性地以犬為模型,系統(tǒng)闡釋衰老及相關認知障礙的分子機制,不僅推動了犬作為人類AD轉化模型的應用,也為解析AD機制提供了關鍵依據。通過系統(tǒng)解析認知障礙犬模型中膠質細胞在生理衰老與CCD病理狀態(tài)下的差異,研究團隊為犬認知障礙的早期干預提供了理論基礎,并為區(qū)分年齡相關認知衰退與CCD特異性病理進程提供了依據。研究成果有望為老年癡呆早期診斷提供潛在分子標志物,并為其發(fā)病機制解析提供重要細胞機制參考。